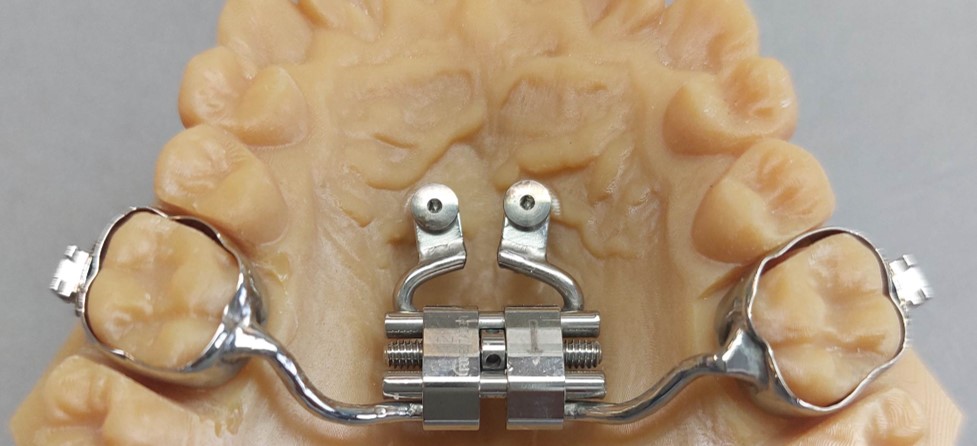
Scuola – lavoro a Padova: collaborazione CNA e IISE Ruzza per la formazione degli allievi odontotecnici
CNA e Istituto Usuelli Ruzza di Padova, in collaborazione, stanno sviluppando un progetto mirato ad offrire agli allievi odontotecnici integrazioni didattiche di aggiornamento. Diversi i relatori impegnati su temi specifici, nel periodo marzo – giugno 2024....Protetto: Elaborazioni a supporto delle imprese per l’applicazione del MDR 745/2017
Protetto da Password
Per visualizzare questo articolo protetto, inserisci qui sotto la password :

Fabbricanti DM su misura: sul portale del Ministero ora è possibile aggiornare i dati inseriti durante la registrazione
Fabbricanti DM su misura: sul portale del Ministero ora è possibile aggiornare i dati inseriti durante la registrazione Dal 28 marzo è possibile aggiornare le informazioni riguardanti i dati identificativi del fabbricante e l’elenco dei tipi di dispositivi medici su...