
da Sandro Storelli | Ott 3, 2025 | Atti, Evoluzione normativa Medicale Veneto, In evidenza, Medicale Veneto, News, Uncategorized
WEBINAR 6.10.2025 Filiera dell’ottica tra innovazione e adeguamento normativo PROGRAMMA SLIDES RELATORI QUALITA’ DELLA VISIONE E CONFORMITA’ S.Storelli, Coordinatore OBV FILIERA OTTICA E MDR745 M.Crosato, Avvocato esperto in sanità MDR 745 –...

da Sandro Storelli | Set 20, 2025 | Eventi, In evidenza, Medicale Veneto
Due giornate di incontri con qualificati operatori internazionali Circular Medical Expo offre agli operatori un’esclusiva opportunità di networking per potenziare le relazioni commerciali e favorire nuove collaborazioni di business. Il format prevede un’area...
da Sandro Storelli | Set 4, 2025 | News
Il 12 settembre 2025 diventa pienamente efficace il Regolamento UE 2023/2854: c.d. Data Act. Il nuovo regolamento si applica anche al settore dei Dispositivi Medici, in tutti i casi in cui il dispositivo raccolga o generi dati relativi al suo utilizzo e sia in grado...
da Sandro Storelli | Ago 29, 2025 | Eventi, Medicale Veneto, News
WEBINAR A PARTECIPAZIONE LIBERA Filiera dell’ottica tra innovazione e adeguamento normativo lunedì 6 ottobre 2025 ore 17.00 Link per partecipare: meet.google.com/goz-frie-uuv PROGRAMMA … — — Il Regolamento UE 2017/745 (MDR) disciplina...
da Sandro Storelli | Ago 26, 2025 | Eventi, Filiera Dentale, In evidenza
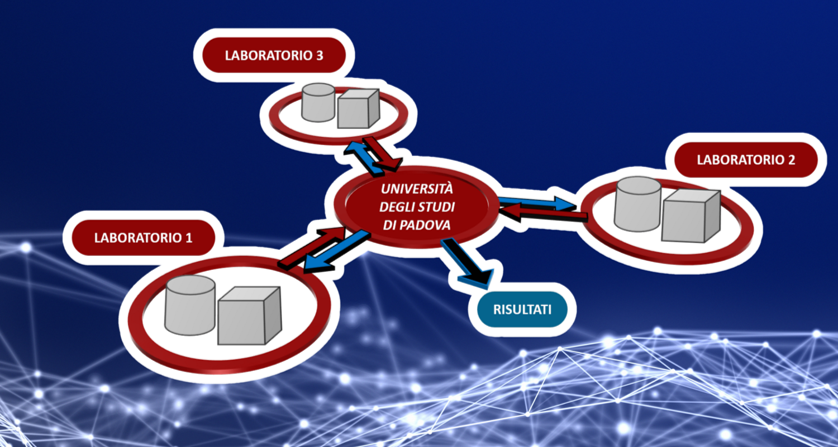
WEBINAR Studio sull’affidabilità delle tecnologie additive nel settore biomedicale Piattaforma web dedicata e raccolta dati del settore PROGRAMMA Webinar SLIDES Sandro Storelli, OBV SLIDES M.Meneghello, E.Vargiu, DGR Università Padova Lo studio, dedicato alle...




