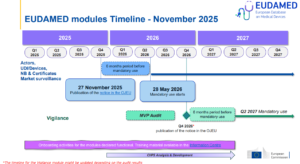
Dal 27 novembre 2025 è operativo il servizio di registrazione in EUDAMED, con la pubblicazione della Decisione (UE) 2025/2371 della Commissione Europea nella Gazzetta Ufficiale UE.
EUDAMED ha concesso un periodo di tempo di 6 mesi per la transizione e i quattro nuovi moduli chiave saranno obbligatori dal 28 maggio 2026 (27.11.2026 per i “Legacy Devices” già conformi alla Direttiva 93/42/CEE e al Regolamento UE 2023/607).
Dal 28 maggio 2026, l’uso dei moduli diventerà obbligatorio per i soggetti rientranti negli ambiti di applicazione del MDR 2017/745 e dell’IVDR 2017/746.
I moduli di registrazione EUDAMED operativi dal 28 maggio 2026 sono:
1. Registrazione degli operatori economici (“Attori”)
2. Banca dati UDI e registrazione dei dispositivi (“UDI e Dispositivi”)
3. Organismi notificati e certificati
4. Sorveglianza del mercato
Ministero della Salute italiano: periodo transitorio e doppia opzione
In questo contesto, il Ministero della Salute italiano è intervenuto per chiarire le modalità operative sul territorio nazionale in un comunicato aggiornato al 15 gennaio 2026 nel sito internet istituzionale.
Fino alla data di utilizzo obbligatorio di uno o più moduli di EUDAMED, si continuano ad applicare le corrispondenti disposizioni delle previgenti direttive.
Il Ministero sottolinea che il Decreto legislativo 5 agosto 2022, n.137 (articolo 31, comma 5) non prevede l’utilizzo obbligatorio della Banca Dati Nazionale dei dispositivi medici nel periodo che intercorre tra la pubblicazione in Gazzetta dell’avviso di funzionalità di un modulo EUDAMED e la data in cui il suo utilizzo diventa effettivamente obbligatorio.
CONSEGUENZA PRATICA: viene introdotta una fase di “doppia opzione”.
Fino alla data in cui l’utilizzo dei primi quattro moduli di Eudamed diventerà obbligatorio, i soggetti tenuti alla registrazione (inclusi gli Organismi Notificati) possono optare per la registrazione o nella Banca dati nazionale (in Italia Repertorio del Ministero della Salute per le forniture agli enti pubblici ospedalieri) o in EUDAMED. I fabbricanti e i mandatari che scelgono l’opzione EUDAMED, dovranno indicare l’Italia tra i Paesi in cui il dispositivo viene commercializzato all’interno del sistema EUDAMED, garantendo così la tracciabilità per il mercato italiano.
Il quadro nazionale: l’articolo 32 del D.Lgs. 137/2022 e la proroga di due anni
Il Decreto legislativo 5 agosto 2022, n. 137, all’articolo 32 comma 4 stabilisce che le lettere a) e b) del comma 1 (che riguardano gli obblighi di registrazione nazionale) sono abrogate decorsi ventiquattro mesi dalla data di pubblicazione dell’avviso di cui all’articolo 34, paragrafo 3, del regolamento (UE) 2017/745 .
Ciò significa che, anche dopo che la Commissione Europea avrà pubblicato l’avviso di funzionalità di EUDAMED, la Banca Dati Nazionale italiana resterà pienamente operativa e vincolante per altri due anni. Questa disposizione offre un periodo di comfort per gli operatori, consentendo una migrazione graduale e pianificata verso il sistema europeo, senza il timore di un “vuoto normativo” o di una sovrapposizione immediata di obblighi.

