da Sandro Storelli | Apr 15, 2020 | Approfondimenti
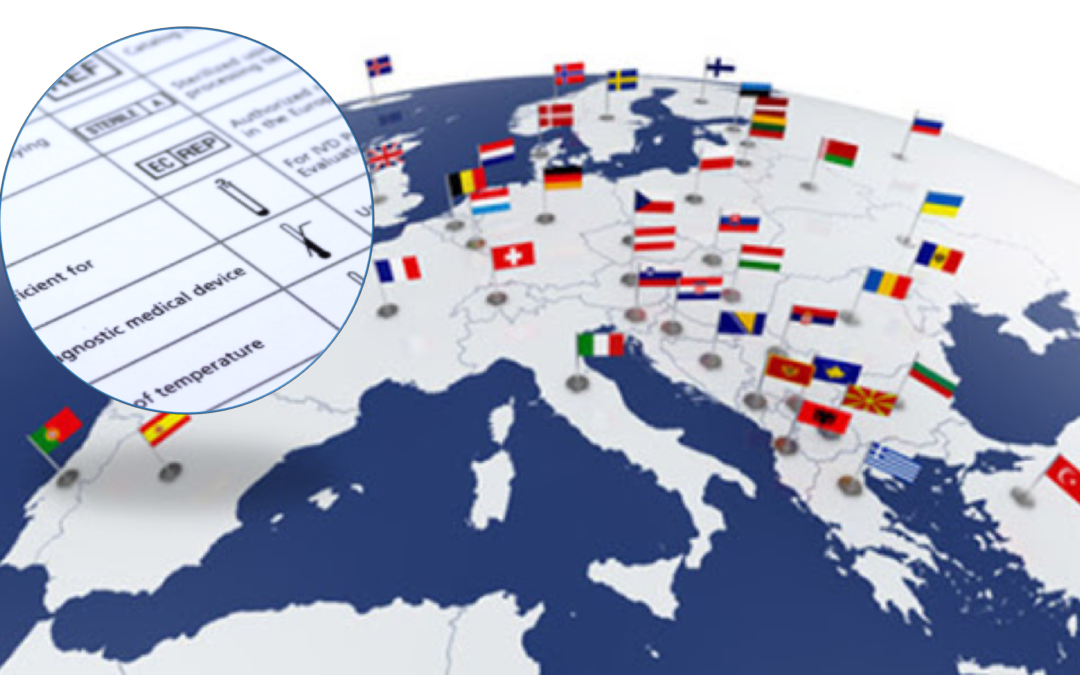
QUESITO: Esiste una norma armonizzata al MDR 2017/745 sui simboli da utilizzare per l’etichettatura dei DM? Se non esiste, come possiamo rendere l’etichetta conforme al Regolamento? RISPONDONO: Gianluca Salerio, Area Normazione internazionale UNI; Sandro...
da Sandro Storelli | Apr 15, 2020 | Approfondimenti
Quesito: CHI TRA FABBRICANTE E MANDATARIO, IN BASE AL MDR 2017/745, DEVE OCCUPARSI DELLA TRADUZIONE DELLE ISTRUZIONI PER L’USO E DELL’ETICHETTA DI UN DISPOSITIVO MEDICO MESSO IN SERVIZIO O IMMESSO IN UNO STATO UE O EXTRA UE (DIVERSO DA QUELLO DEL FABBRICANTE)? (Un...
da Sandro Storelli | Apr 15, 2020 | Approfondimenti
DOMANDA: L’odontotecnico che lo fabbrica deve dichiarare quanto dura la vita del DM su misura? Per quanto tempo ne è responsabile? Risponde Sandro Storelli, esperto senior di aspetti regolatori nel medicale RISPOSTA: I dispositivi medici dentali, fabbricati dal...
da Sandro Storelli | Mar 3, 2020 | Approfondimenti, Fabbricante odontotecnico
Sicurezza biologica – In queste settimane, dal punto di vista mediatico, il COVID19 è stato il tema predominante. La prima settimana di emergenza ha insegnato, tra l’altro, che le informazioni devono essere adeguatamente mediate, per non far scattare inutili e...



